Note : Les descriptions sont présentées dans la langue officielle dans laquelle elles ont été soumises.
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
1
PROCEDE D'EXTRACTION LIQUIDE - LIQUIDE POUR LA PURIFICATION DE L'URANIUM
ISSU DE LA DISSOLUTION NITRIQUE D'UN CONCENTRE D'URANIUM NATUREL
DESCRIPTION
DOMAINE TECHNIQUE
La présente invention se rapporte à un
procédé permettant de purifier l'uranium d'un concentré
d'uranium naturel.
Elle trouve application dans le domaine du
raffinage des concentrés d'uranium naturel qui sont
produits par les mines d'uranium et dont l'uranium
qu'ils renferment est notamment destiné, après
purification, à être converti soit en uranium métal,
soit en composés d'uranium comme, par exemple, en
hexafluorure d'uranium (ou UF6), en tétrafluorure
d'uranium (ou UF4), en dioxyde d'uranium (ou U02) ou en
octooxyde de triuranium (U308), qui sont des produits
intermédiaires de la fabrication des combustibles
nucléaires.
ÉTAT DE LA TECHNIQUE ANTÉRIEURE
Les usines de raffinage des concentrés
d'uranium naturel utilisent, pour amener l'uranium
contenu dans ces concentrés à une pureté dite
nucléaire , un procédé qui comprend, après
dissolution desdits concentrés dans de l'acide nitrique
pour obtenir une solution aqueuse de nitrate d'uranyle
impur .
- l'extraction de ce nitrate par une phase
organique contenant un extractant très affine pour lui,
dans un diluant organique, puis
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
2
- le lavage de la phase organique obtenue
à l'issue de cette extraction, par une phase aqueuse en
vue d'éliminer de la phase organique les espèces
chimiques indésirables susceptibles d'avoir été
extraites avec le nitrate d'uranyle, et
- la désextraction du nitrate d'uranyle de
la phase organique ainsi lavée, de manière à récupérer
le nitrate d'uranyle dans une phase aqueuse.
Ces trois opérations sont effectuées dans
des appareils d'extraction liquide-liquide, par exemple
des colonnes agitées.
L'extractant utilisé est le phosphate de
tri-n-butyle (ou TBP) qui est également employé comme
extractant dans le traitement des combustibles
nucléaires irradiés et qui a été choisi par tous les
raffineurs comme étant le mieux adapté aux contraintes
de sélectivité, de solubilité dans l'eau, de stabilité
chimique, de densité, de corrosion, de toxicité et de
sécurité imposées par le procédé.
Néanmoins, ce procédé de purification
présente un certain nombre d'inconvénients qui sont
inhérents à l'utilisation de cet extractant.
Le premier de ces inconvénients est qu'il
se produit, dans l'appareil dans lequel est effectuée
l'opération d'extraction, une accumulation de thorium
(impureté présente dans les minerais d'uranium) qui est
due à une boucle d'extraction-désextraction de cet
élément dans cet appareil. En effet, le thorium étant
lui aussi extractible par le TBP, il est extrait dans
la zone de l'appareil où la phase organique présente
une faible concentration en nitrate d'uranyle puis
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
3
désextrait de cette phase dans la zone de l'appareil où
la phase organique est saturée en nitrate d'uranyle.
Cette accumulation de thorium provoque un
pic de débit de dose dû à l'irradiation générée par le
protactinium 234 métastable (234mPa), après décroissance
du thorium 234 présent dans la solution de nitrate
d'uranyle impur, qui est un descendant direct de
l'uranium 238.
Pour éviter la survenue d'un tel pic de
débit de dose, il est connu d'ajouter à la solution de
nitrate d'uranyle impur des agents capables de
complexer le thorium au cours de l'opération
d'extraction, lesquels peuvent être des fluorures ou
des phosphates. Toutefois, la présence de ces agents
complexants dans les effluents aqueux produits ajoute
des contraintes d'exploitation du procédé et de gestion
de ces effluents, du type pollution de l'acide nitrique
régénéré et des distillats, corrosion des matériels
utilisés, précipitations, etc.
Un autre inconvénient est que l'opération
de désextraction est relativement difficile à réaliser
en raison d'une extraction non négligeable de l'uranium
par le TBP, même à faible acidité. Il est donc
nécessaire de chauffer à au moins 50 C la phase aqueuse
que l'on utilise pour réaliser cette opération,
typiquement de l'eau distillée, et d'utiliser des
débits aqueux importants pour obtenir une désextraction
quantitative du nitrate d'uranyle.
Outre que l'utilisation d'une phase aqueuse
présentant une température d'au moins 50 C est
pénalisante pour la sécurité des installations en
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
4
raison des risques d'inflammabilité de la phase
organique, l'utilisation de débits aqueux importants se
traduit par une dilution importante du nitrate
d'uranyle. Ainsi, alors que la concentration du nitrate
d'uranyle est initialement de l'ordre de 400 g/L dans
la solution de nitrate d'uranyle impur, elle est au
mieux de 130 g/L dans la phase aqueuse issue de
l'opération de désextraction. La phase organique
saturée en uranium contient environ 150 g/L d'uranium
en sortie d'extraction. Pour éviter les fuites
d'uranium dans cette phase organique, le rapport
maximal des débits 0/A (organique sur aqueux) à la
désextraction est inférieur à 1 (de l'ordre de 0,8)
même à 60 C.
La désextraction n'étant pas assez
concentrante, il est donc nécessaire de soumettre
ensuite cette phase aqueuse à une opération de
concentration, coûteuse en énergie avant traitement
ultérieur par dénitration.
Enfin, en raison de la solubilité non
négligeable du TBP en phase aqueuse acide, il serait
nécessaire de laver les effluents aqueux des opérations
d'extraction et lavage avec du diluant organique pour
récupérer le TBP présent dans ces effluents et éviter
de la sorte une surconsommation d'extractant.
Compte tenu de ce qui précède, les
Inventeurs se sont donc fixé pour but de fournir un
procédé qui, tout en permettant de purifier très
efficacement la totalité de l'uranium contenu dans un
concentré d'uranium naturel, soit exempt des
inconvénients mentionnés ci-dessus.
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
EXPOSÉ DE L'INVENTION
Ce but et d'autres encore sont atteints par
la présente invention qui propose un procédé permettant
de purifier l'uranium d'un concentré d'uranium naturel
5 contenant au moins l'une des impuretés suivantes :
thorium, molybdène, zirconium, fer, calcium et
vanadium, lequel procédé comprend :
a) l'extraction de l'uranium présent sous
la forme de nitrate d'uranyle dans une phase aqueuse Al
résultant de la dissolution dudit concentré d'uranium
naturel dans de l'acide nitrique, par mise en contact
de cette phase aqueuse avec une phase organique non
miscible à l'eau, qui contient un extractant dans un
diluant organique, puis séparation desdites phases
aqueuse et organique ;
b) le lavage de la phase organique obtenue
à l'issue de l'étape a), par mise en contact de cette
phase organique avec une phase aqueuse A2 puis
séparation desdites phases organique et aqueuse ; et
c) la désextraction du nitrate d'uranyle de
la phase organique obtenue à l'issue de l'étape b),
cette désextraction étant réalisée par circulation de
cette phase organique dans un appareil, à contre-
courant d'une phase aqueuse A3, puis séparation
desdites phases organique et aqueuse ;
et est caractérisé en ce que, d'une part,
l'extractant contenu dans la phase organique est un
N,N-dialkylamide et, d'autre part, le rapport entre les
débits auxquels circulent la phase organique obtenue à
l'issue de l'étape b) et la phase aqueuse A3 dans
l'appareil où se déroule l'étape c) est supérieur à 1
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
6
de sorte que la désextraction du nitrate d'uranyle
s'accompagne d'une concentration de ce nitrate.
Ainsi, le procédé de l'invention reprend
les trois principales opérations (extraction, lavage,
désextraction) du procédé de purification de l'art
antérieur mais utilise un N,N-dialkylamide comme
extractant, au lieu du TBP.
Il est à noter que l'utilisation d'une
phase organique contenant un N,N-dialkylamide pour
extraire de l'uranium d'une phase aqueuse dans laquelle
il se trouve n'est pas nouvelle en soi. Ainsi, par
exemple, elle a été proposée pour extraire l'uranium
et/ou le plutonium présents dans des solutions aqueuses
résultant de la dissolution de combustibles nucléaires
irradiés (demande de brevet français publiée sous le
numéro 2 642 562 [2]) ainsi que pour extraire l'uranium
présent dans des solutions aqueuses concentrées en
thorium car produit par irradiation de ce thorium
(demande de brevet français publiée sous le
numéro 2 642 561 [2]).
Ce qui, par contre, est tout à fait nouveau
est le fait d'utiliser une phase organique contenant un
N,N-dialkylamide pour purifier l'uranium d'un concentré
minier uranifère, et ce qui est inattendu est que cette
utilisation permette à la fois :
- d'éviter l'accumulation du thorium
observée lorsque l'opération d'extraction est réalisée
au moyen d'une phase organique contenant du TBP et, par
là même, de supprimer la nécessité d'employer des
agents complexants avec tous les avantages qu'implique
cette suppression, en particulier en termes de
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
7
simplification de l'exploitation du procédé et de la
gestion des effluents aqueux générés ;
- de réaliser l'opération de désextraction
à des températures plus faibles que celles utilisées
dans le procédé de purification de l'art antérieur,
même si elle peut néanmoins être réalisée à des
températures de 50 à 60 C, et en utilisant des débits
de phase aqueuse inférieurs à ceux qui sont nécessaires
lorsque la phase organique contient du TBP, et, par là
même, d'alléger l'opération ultérieure de concentration
avec, là également, tous les avantages que cet
allégement implique, en particulier en termes
d'économies d'énergie ;
- de limiter les pertes d'extractant en
phase aqueuse en raison de la faible solubilité des
N,N-dialkylamides en phase aqueuse, et de faciliter le
traitement des raffinats d'extraction pour recycler
l'acide nitrique dans le procédé.
Comme N,N-dialkylamides, on peut notamment
utiliser ceux qui répondent à la formule (I) ci-après
R2
/(CH2) a- CH -R3
R1-C -N
Il (CH2) b- CH -R5
14
R (I)
dans laquelle
- R1 représente un groupe alkyle, ramifié en alpha
ou bêta du groupe carbonyle et comprenant de 3 à 12
atomes de carbone ;
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
8
- R2 et R4, qui peuvent être identiques ou
différents, représentent un groupe alkyle, linéaire ou
ramifié et comprenant de 2 à 4 atomes de carbone ;
- R3 et R5, qui peuvent être identiques ou
différents, représentent un groupe alkyle, linéaire ou
ramifié et comprenant de 1 à 6 atomes de carbone ; et
- a et b, qui peuvent être identiques ou
différents, sont des nombres entiers allant de 1 à 6.
Parmi ces N,N-dialkylamides, on préfère
utiliser ceux dans lesquels a et b valent tous les deux
1 et dans lesquels R2 et R4 représentent tous les deux
un groupe éthyle comme le N,N-di-(2-éthylhexyl)-
isobutyramide (ou DEHiBA, dans lequel R1 = -CH(CH3)2 et
R3 = R5 = - (CH2) 3CH3) , le N, N-di- (2-éthylhexyl) -2, 2-
diméthylpropanamide (ou DEHDMPA, dans lequel
R1 = -C (CH3) 3 et R3 = R5 = - (CH2) 3CH3) ou encore le N, N-
di-(2-éthylhexyl)-3,3-diméthylbutanamide (ou DEHDMBA,
dans lequel R1 = -CH2C (CH3) 3 et R3 = R5 = - (CH2) 3CH3) , le
DEHiBA étant tout particulièrement préféré.
Quant au diluant organique, il s'agit, de
préférence, d'une isoparaffine ou d'un mélange
d'isoparaffines dont la chaîne carbonée comprend de 9 à
13 atomes de carbone du type de celles commercialisées
par la société TOTAL sous la référence commerciale
Isane IP 185.
Toutefois, on peut également utiliser
d'autres diluants organiques aliphatiques tels que le
kérosène ou un dodécane, linéaire ou ramifié, comme le
n-dodécane ou le tétrapropylène hydrogéné (ou TPH).
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
9
Dans tous les cas, la concentration du
N,N-dialkylamide dans le diluant organique est, de
préférence, de 1 à 2 moles/L.
La phase aqueuse Al contient, de
préférence, de 0,5 à 4 moles/L d'acide nitrique.
La phase aqueuse A2 est, de préférence, de
l'eau, préférentiellement distillée, ou une solution
aqueuse contenant de 0,01 à 1,5 mole/L d'acide nitrique
ou bien encore une fraction de la phase aqueuse obtenue
à l'issue de l'étape c).
Quant à la phase aqueuse A3, elle est soit
de l'eau, préférentiellement distillée, soit une
solution aqueuse d'acide nitrique faiblement
concentrée, c'est-à-dire ne contenant, de préférence,
pas plus de 0,01 mole/L d'acide nitrique.
Conformément à l'invention, cette phase
aqueuse A3 peut être utilisée à la température
ambiante, c'est-à-dire à une température allant
typiquement de 20 à 25 C, mais elle peut aussi être
chauffée à une température de 50 à 60 C comme dans le
procédé de purification de l'art antérieur.
Comme précédemment indiqué, à l'étape c),
le rapport entre les débits auxquels circulent la phase
organique obtenue à l'issue de l'étape b) et la phase
aqueuse A3 dans l'appareil où se déroule l'étape c) est
supérieur à 1 et, de préférence, égal ou supérieur à
1, 5.
Le procédé de l'invention peut être mis en
oeuvre dans tous les types d'appareils classiquement
utilisés dans le domaine des extractions liquide-
liquide tels que des batteries de mélangeurs-
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
décanteurs, des colonnes pulsées ou agitées, des
extracteurs centrifuges, etc.
Outre les avantages précédemment
mentionnés, le procédé de l'invention présente encore
5 d'autres avantages comme le fait que, d'une part, les
produits de dégradation des N,N-dialkylamides sont
beaucoup moins gênants que les produits de dégradation
du TBP et, en particulier, le phosphate de di-n-butyle
qui complexe très fortement certains cations
10 métalliques, et, d'autre part, les N,N-dialkylamides
sont totalement incinérables car uniquement constitués
d'atomes de carbone, d'oxygène, d'azote et d'hydrogène,
ce qui n'est pas le cas du TBP.
D'autres caractéristiques et avantages de
l'invention ressortiront du complément de description
qui suit et qui se rapporte à des essais expérimentaux
ayant permis de valider le procédé de l'invention.
Il va de soi que ce complément de
description n'est donné qu'à titre d'illustration de
l'objet de l'invention et ne doit en aucun cas être
interprété comme une limitation de cet objet.
BREVE DESCRIPTION DES FIGURES
La figure 1 illustre schématiquement un
premier essai de mise en oeuvre du procédé de
l'invention en batteries de mélangeurs-décanteurs.
La figure 2 montre les valeurs du
coefficient de distribution du thorium 234, noté DTh,
telle qu'observées au cours d'essais en tubes
consistant à épuiser une solution aqueuse d'uranium,
contenant 2 moles/L d'acide nitrique, au moyen de cinq
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
11
phases organiques contenant soit du DEHiBA soit du TBP
dans de l'Isane IP 185.
La figure 3 illustre schématiquement un
autre essai de mise en oeuvre du procédé de l'invention
en batteries de mélangeurs-décanteurs.
La figure 4 montre les profils des
concentrations de l'uranium en phases aqueuse et
organique telles qu'obtenues expérimentalement et par
calculs dans les différents étages des mélangeurs-
décanteurs utilisés dans l'essai illustré sur la figure
3.
EXPOSÉ DÉTAILLÉ DE L'INVENTION
EXEMPLE 1 :
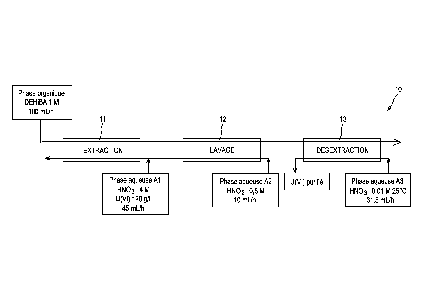
On se réfère tout d'abord à la figure 1 qui
illustre schématiquement un premier essai de mise en
oeuvre du procédé de l'invention en batteries de
mélangeurs-décanteurs.
Cet essai a été réalisé dans une
installation 10 comprenant :
- une première batterie, référencée 11, de
16 mélangeurs-décanteurs, dévolue à l'extraction du
nitrate d'uranyle de la phase aqueuse Al ;
- une deuxième batterie, référencée 12, de
8 mélangeurs-décanteurs, dévolue au lavage de la phase
organique obtenue à l'issue de l'extraction ; et
- une troisième batterie, référencée 13,
de 16 mélangeurs-décanteurs, dévolue à la désextraction
du nitrate d'uranyle de la phase organique obtenue à
l'issue du lavage de cette phase.
Ont été utilisées :
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
12
- comme phase organique : une phase
contenant 1 mole/L de DEHiBA dans du TPH et circulant à
un débit de 100 mL/heure dans les trois batteries de
mélangeurs-décanteurs ;
- comme phase aqueuse Al : une solution à
4 moles/L d'acide nitrique et 120 g/L d'uranium (sous
forme de nitrate d'uranyle), et circulant à un débit de
45 mL/heure dans la batterie 11 ;
- comme phase aqueuse A2 : une solution
d'acide nitrique à 0,5 mole/L, circulant à un débit de
10 mL/heure dans la batterie 12 et s'additionnant à ce
même débit à la phase aqueuse Al dans la batterie 11 ;
et
- comme phase aqueuse A3 : une solution
d'acide nitrique à 0,01 mole/L et circulant à un débit
de 31,5 mL/heure dans la batterie 13.
Les rapports de débits 0/A (organique sur
aqueux) dans les batteries 11, 12 et 13 étaient donc
respectivement de 1,8, de 10 et de 3.
Toutes les phases, y compris la phase
aqueuse A3, ont été utilisées à 25 C.
Après 700 heures de fonctionnement de
l'installation, l'essai a montré qu'il est possible de
récupérer, dans la phase aqueuse sortant de la batterie
13, plus de 99,99% du nitrate d'uranyle initialement
présent dans la phase aqueuse Al et à une concentration
bien supérieure à celle qu'il présente dans la phase
aqueuse Al, à savoir 160 g/L versus 120 g/L, soit un
facteur de concentration de 1,3.
La phase organique sortant de la batterie
12 contient environ 54 g/L d'uranium, qui est
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
13
quantitativement désextrait dans la batterie 13 en
utilisant un rapport de débits O/A de 3 pour obtenir
une solution à 160 g/L d'uranium.
La faible extractibilité de l'uranium par
le DEHiBA, à faible acidité nitrique, rend donc
possible une désextraction concentrante du nitrate
d'uranyle à la température de 25 C, alors qu'elle est
impossible à obtenir si la phase organique contient du
TBP et ce, même en chauffant la phase aqueuse utilisée
pour effectuer cette désextraction.
EXEMPLE 2 :
La solubilité du DEHiBA en phase aqueuse a
été appréciée en effectuant un essai en mélangeurs-
décanteurs similaire à celui décrit dans l'exemple 1
ci-avant et en mesurant le carbone organique total (ou
COT) présent, d'une part, dans la phase aqueuse sortant
de la batterie 11 (ci-après dénommée raffinat
d'extraction ) et, d'autre part, dans la phase aqueuse
sortant de la batterie 13 et contenant le nitrate
d'uranyle purifié (ci-après dénommée production U ).
Le carbone organique total a été mesuré au
moyen d'un COT-mètre thermique dans les phases aqueuses
telles qu'obtenues après décantation, c'est-à-dire sans
soumettre ces phases à une quelconque centrifugation.
Le tableau 1 ci-après présente, pour les
deux phases aqueuses testées, leur acidité, la valeur
du COT obtenue et la conversion de cette valeur en
équivalent DEHiBA, cette conversion ayant été réalisée
en partant de l'hypothèse que tout le carbone organique
présent dans les phases aqueuses est issu de cet
extractant.
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
14
TABLEAU 1
Phase aqueuse Raffinat Production U
d'extraction
HN03 (moles/L) 3,1 0,34
COT (mg/L) 31 46
Equivalent
DEHiBA 1, 3.10-4 1, 9.10-4
(moles/L)
Ce tableau montre qu'environ 40 à 60 mg/L
de DEHiBA seraient solubles en phase aqueuse dans les
conditions de l'essai.
Ces valeurs de solubilité sont supérieures
à la solubilité du DEHiBA en phase aqueuse annoncée
dans la littérature par Al-Jallo et al. (J. Chem. Eng.
Data 1984, 29, 479-481 [3]) et par Gasparini et Grossi
(Separation Science and Technology 1980, 15(4), 825-844
[4]) mais elles englobent la solubilité de l'extractant
lui-même, celle du diluant organique (TPH) ainsi que
les phénomènes d'entrainement non négligeables de la
phase organique dans les solutions aqueuses en sortie
de la batterie de mélangeurs-décanteurs.
Ces valeurs de solubilité restent néanmoins
inférieure à la solubilité intrinsèque du TBP dans les
mêmes conditions, qui est de 200 à 300 mg/L, et
confirment que les pertes d'extractant en phase aqueuse
sont beaucoup plus faibles dans le cas où la phase
organique contient du DEHiBA.
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
EXEMPLE 3
La sélectivité du DEHiBA pour l'uranium
vis-à-vis des impuretés qui sont majoritairement
présentes dans les concentrés naturels d'uranium ou qui
5 sont pénalisantes dans les étapes ultérieures de
conversion et d'enrichissement de l'uranium a également
été appréciée en réalisant deux séries d'essais.
La première série d'essais a consisté à
déterminer les coefficients de distribution du
10 thorium(IV), du molybdène(VI), du zirconium(IV), du
fer(III), du calcium(II) et du vanadium(V) à l'issue
d'un seul contact en tubes entre une phase solvant
contenant 1,5 mole/L de DEHiBA dans de l'Isane IP 185
et des solutions aqueuses nitriques contenant ces
15 cations, en présence ou non de 30 g/L d'uranium, et
présentant différentes acidités (de 0,5 à 4 M).
Pour chaque essai, les phases aqueuse et
organique ont été mises en contact volume à volume et
laissées sous agitation pendant 1 heure, à une
température constante de 25 C. Puis, après décantation
et séparation de ces phases, la concentration en
cations a été déterminée dans la phase aqueuse et dans
la phase organique par spectrométrie d'émission
atomique (ou ICP-AES).
Cette première série d'essais a permis de
mettre en évidence qu'avec ou sans uranium et dans la
gamme d'acidités nitriques étudiée, les coefficients de
distribution du molybdène, du zirconium, du fer, du
calcium et du vanadium sont inférieurs à 10-3 et
conduisent à des facteurs de séparation U/impuretés
supérieurs à 10 000, soit largement suffisants pour
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
16
atteindre les spécifications de la norme ASTM C 788 en
termes de purification du nitrate d'uranyle.
Le coefficient de distribution du
thorium(IV) est également très faible (inférieur à
5.10-3) pour une teneur en acide nitrique de 4 moles/L
et ce, quelle que soit la concentration en uranium de
la phase aqueuse, confirmant la forte sélectivité du
DEHiBA pour l'uranium vis-à-vis du thorium(IV).
La deuxième série d'essais a consisté à
épuiser une solution aqueuse contenant 360 g/L
d'uranium et 2 moles/L d'acide nitrique en mettant
cette solution aqueuse en contact, en tubes, avec
successivement cinq phases organiques contenant soit
1,5 mole/L de DEHiBA soit du TBP à 36% (v/v) dans de
l'Isane IP 185 et à déterminer, après chaque contact,
le coefficient de distribution du thorium 234 issu de
la décroissance de l'uranium 238.
Pour les deux premiers contacts, les phases
aqueuse et organique ont été utilisées à raison d'un
volume de phase aqueuse pour deux volumes de phase
organique, tandis que pour les trois derniers contacts,
les phases aqueuse et organique été utilisées volume à
volume. Dans tous les cas, les phases aqueuse et
organique ont été laissées sous agitation pendant 10
minutes à une température constante de 25 C.
Après décantation et séparation des phases
aqueuse et organique, l'activité du thorium 234 a été
déterminée dans chacune de ces phases par spectrométrie
7-
Les résultats de cette deuxième série
d'essais sont illustrés sur la figure 2 qui montre les
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
17
valeurs du coefficient de distribution du thorium 234,
noté DTh, obtenues à l'issue de chaque contact et pour
les deux types de phases organiques.
Cette figure montre que, dans le cas où les
phases organiques contiennent du TBP, DTh devient
supérieur à 1 après le 3eme contact, c'est-à-dire après
épuisement de la phase aqueuse en uranium, alors que,
dans le cas où les phases organiques contiennent du
DEHiBA, DTh se maintient à une valeur inférieure à 10-2
même après épuisement de la phase en uranium.
Ainsi, l'accumulation de thorium, qui se
produit dans l'appareil d'extraction dans le procédé de
purification de l'art antérieur et que les essais
décrits ci-dessus ont permis de simuler, ne devrait pas
se produire dans le procédé de l'invention.
EXEMPLE 4 :
On se réfère à présent à la figure 3 qui
illustre schématiquement un autre essai de mise en
oeuvre du procédé de l'invention en batteries de
mélangeurs-décanteurs.
Cet essai a été réalisé dans une
installation 20 comprenant :
- une première batterie, référencée 21, de
8 mélangeurs-décanteurs, dévolue à l'extraction du
nitrate d'uranyle de la phase aqueuse Al ;
- une deuxième batterie, référencée 22, de
8 mélangeurs-décanteurs, dévolue au lavage de la phase
organique obtenue à l'issue de l'extraction ; et
- une troisième batterie, référencée 23,
de 8 mélangeurs-décanteurs, chauffée à 50 C, dévolue à
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
18
la désextraction du nitrate d'uranyle de la phase
organique obtenue à l'issue du lavage de cette phase.
Ont été utilisées :
- comme phase organique : une phase
contenant 1,5 mole/L de DEHiBA dans du TPH et circulant
à un débit de 145 mL/heure dans les trois batteries de
mélangeurs-décanteurs ;
- comme phase aqueuse Al : une solution
contenant 1,5 mole/L d'acide nitrique, 435 g/L
d'uranium (sous forme de nitrate d'uranyle), environ
5400 kBq/L (soit 6 ng/L) de thorium 234 issu de la
décroissance de l'uranium 238 ainsi que des impuretés
caractéristiques (736 mg/L de fer, 359 mg/L de
molybdène, 258 mg/L de zirconium, 34 mg/L de vanadium
et 106 mg/L de calcium), et circulant à un débit de
50 mL/heure dans la batterie 21 ;
- comme phase aqueuse A2 : une fraction de
la solution sortant de la batterie 23, circulant à un
débit de 6 mL/heure dans la batterie 22 et
s'additionnant à ce même débit à la phase aqueuse Al
dans la batterie 21 ; et
- comme phase aqueuse A3 : une solution
d'eau distillée chauffée et circulant à un débit de
75 mL/heure dans la batterie 23.
Les rapports de débits O/A (organique sur
aqueux) dans les batteries 21, 22 et 23 étaient donc
respectivement de 2,6, de 24 et de 1,9.
Après 24 heures de fonctionnement de
l'installation, l'essai a montré qu'il est possible de
récupérer, dans la phase aqueuse sortant de la batterie
23, plus de 99% du nitrate d'uranyle initialement
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
19
présent dans la phase aqueuse Al et à une concentration
de 281,5 g/L, soit bien supérieure à la concentration
d'uranium récupérée dans le procédé de purification de
l'art antérieur (130 g/L). Les pertes d'uranium dans la
phase aqueuse sortant de la batterie 21 ont été
estimées à 0,2 mg/L.
Le thorium 234, dosé par spectrométrie y, se
retrouve quantitativement dans la phase aqueuse sortant
de la batterie 21 (c'est-à-dire que 100% du thorium
initial sont récupérés à l'issue de l'essai) et ne
s'accumule pas dans cette batterie et ce, sans avoir
recours à un complexant spécifique, confirmant ainsi la
sélectivité du DEHiBA pour l'uranium par rapport au
thorium.
La phase organique sortant de la batterie
22 contient environ 156 g/L d'uranium, qui est
quantitativement désextrait dans la batterie 23 en
utilisant un rapport de débits 0/A de 1,9 pour obtenir
une solution à 281,5 g/L d'uranium.
L'essai a, par ailleurs, montré que le
nitrate d'uranyle était suffisamment décontaminé vis-à-
vis des principales impuretés présentes dans les
concentrés miniers. Les résultats ont montré la
présence de traces de fer, molybdène, zirconium et
calcium inférieures au mg/L dans la solution purifiée
de nitrate d'uranyle et n'ont pas détecté la présence
de vanadium. Le thorium mesuré dans le nitrate
d'uranyle purifié à une concentration de 8.10-14 g/L est
probablement dû à la re-création de thorium dans
l'échantillon d'uranium par décroissance de cet uranium
et confirme les coefficients de distribution très
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
faibles du thorium que l'on obtient avec une phase
organique contenant du DEHiBA.
Ces valeurs sont répertoriées dans le
tableau 2 ci-après et comparées aux spécifications de
5 la norme ASTM C 788.
TABLEAU 2
Impuretés dans la
solution de nitrate Mo V Zr Ca Fe
d'uranyle purifiée
Spécifications
ASTM C 788 1,4 1,4 Somme < 500
( g/g d'uranium)
Essai en mélangeurs-
décanteurs 1,1 < 1 3,6 2,7 3
( g/g d'uranium)
Par ailleurs, la figure 4 montre les
10 profils des concentrations de l'uranium, exprimées en
g/L, en phases aqueuse et organique, telles qu'obtenues
expérimentalement et par calculs, dans les différents
étages des mélangeurs-décanteurs.
Sur cette figure, [U (VI) ] aq. exp. correspond
15 aux concentrations de l'uranium en phase aqueuse
expérimentales ; [U(VI)]orq. exp. correspond aux
concentrations de l'uranium en phase organique
expérimentales ; [U(VI)1aq. calc. correspond aux
concentrations de l'uranium en phase aqueuse calculées
20 tandis que [U(VI)]orq. calc. correspond aux
CA 02785001 2012-06-19
WO 2011/076739 PCT/EP2010/070248
21
concentrations de l'uranium en phase organique
calculées.
Le bon accord entre les valeurs
expérimentales et calculées confirme la validité du
modèle d'extraction de l'uranium par le DEHiBA élaboré
pour simuler le procédé de l'invention.
L'utilisation du DEHiBA permet donc de
récupérer la totalité de l'uranium présent en solution,
à une concentration deux fois plus élevée que celle qui
est actuellement obtenue industriellement avec le TBP
et suffisamment décontaminé des principales impuretés
cationiques présentes dans les concentrés miniers et
gênantes pour les opérations ultérieures
d'enrichissement tout en évitant l'accumulation du
thorium à l'étape d'extraction.
REFERENCES CITEES
[1] demande de brevet français n 2 642 562
[2] demande de brevet français n 2 642 561
[3] Al-Jallo et al., J. Chem. Eng. Data 1984, 29, 479-
481
[4] Gasparini et Grossi, Separation Science and
Technology 1980, 15(4), 825-844